Ostatnia aktualizacja:
| Substancja czynna | Ceftiofur |
| Postać farmaceutyczna | Brak danych |
| Podmiot odpowiedzialny | |
| Kod ATC | |
| Procedura | |
| Kategorie | C, Leki stosowane u bydła, Leki stosowane u świń |
Spis treści
- 1 Jakie są wskazania? Na co stosowany jest Cefur?
- 2 Jaki jest skład Cefur, jakie substancje zawiera?
- 3 Jak dawkować Cefur?
- 4 Jakie są zalecenia dla prawidłowego podania?
- 5 Jakie są przeciwwskazania?
- 6 Jakie są działania niepożądane?
- 7 Jakie są okres(-y) karencji?
- 8 Jakie są specjalne ostrzeżenia dla każdego z docelowych gatunków zwierząt?
- 9 Jakie są specjalne ostrzeżenia dotyczące stosowania u zwierząt?
- 10 Jakie są specjalne środki ostrożności dla osób podających Cefur zwierzętom?
- 11 Jak stosować Cefur w przypadku ciąży, laktacji lub nieśności?
- 12 Czy występują interakcje Cefur z innymi produktami?
- 13 Jak postępować w przypadku przedawkowania?
- 14 Jakie są główne niezgodności farmaceutyczne?
- 15 Aktualna ulotka leku Cefur
- 16 Aktualna charakterystyka produktu leczniczego (ChPL)
Jakie są wskazania? Na co stosowany jest Cefur?
Produkt Cefur zawiera ceftiofur, który jest opornym na działanie beta-laktamaz bakteriobójczym antybiotykiem o szerokim spektrum należącym do grupy cefalosporyn. Produkt jest wskazany do:
1) Leczenia ostrych, bakteryjnych chorób układu oddechowego bydła wywołanych przez wrażliwe na ceftiofur Mannheimia haemolytica, Pasteurella multocida lub Histophilus somni.
2) Leczenia ostrej nekrobacylozy międzypalcowej (zanokcicy) u bydła wywołanej przez Fusobacterium necrophorum i Bacteroides melaninogenicus.
3) Leczenia chorób bakteryjnych układu oddechowego świń wywołanych przez wrażliwe na ceftiofur Actinobacillus (Haemophilus) pleuropneumoniae, Pasteurella multocida i/lub Streptococcus suis.
Jaki jest skład Cefur, jakie substancje zawiera?
Produkt jest proszkiem barwy szarawobiałej do brązowej, pakowanym w fiolki zawierające ceftiofur sodowy w ilości odpowiadającej 1 g lub 4 g ceftiofuru.
Każda fiolka z rozpuszczalnikiem zawiera 20 ml lub 80 ml wody do wstrzykiwań.
Roztwór po rekonstytucji zawiera 50 mg ceftiofuru / ml.
Jak dawkować Cefur?
Przygotowanie roztworu (rekonstytucja)
Fiolka 1g: zawartość rozpuścić poprzez dodanie 20 ml wody do wstrzykiwań.
Fiolka 4g: zawartość rozpuścić poprzez dodanie 80 ml wody do wstrzykiwań.
Wskazówki dotyczące przygotowania roztworu:
1. Usunąć uszczelniającą osłonkę korka z fiolek zawierających proszek i rozpuszczalnik.
2. Pobrać dokładną wymaganą objętość wody do wstrzykiwań używając sterylnej igły 18G i strzykawki.
3. Wstrzyknąć odmierzoną objętość rozpuszczalnika do fiolki z proszkiem.
4. Wstrząsać do momentu pełnego rozpuszczenia proszku.
Najlepsze rezultaty osiąga się po szybkim dodaniu rozpuszczalnika o temperaturze pokojowej. Podczas przygotowywania roztworu, w celu uniknięcia zanieczyszczeń mikrobiologicznych, należy przestrzegać zasad aseptyki.
Dawkowanie u bydła i świń
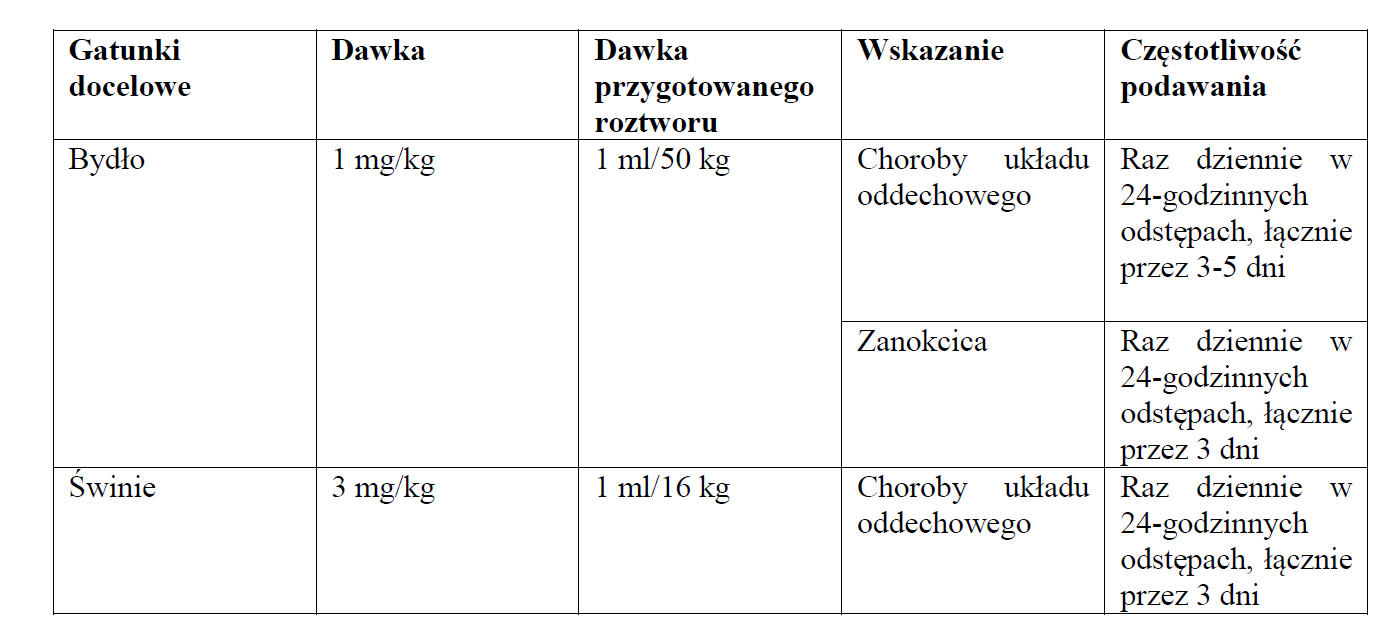
W jedno miejsce iniekcji nie należy podawać więcej niż 10 ml roztworu.
Jakie są zalecenia dla prawidłowego podania?
Należy podawać wyłącznie domięśniowo u bydła i świń. U świń należy zachować szczególną ostrożność, aby uniknąć wstrzyknięcia w tkankę tłuszczową.
Podczas iniekcji należy przestrzegać normalnych zasad aseptyki.
Należy unikać powtórnego wstrzykiwania w to samo miejsce iniekcji.
U świń należy stosować odpowiednio wyskalowane strzykawki w celu podania dawki o dokładnie odmierzonej objętości. Jest to szczególnie istotne przy podawaniu prosiętom o masie ciała poniżej 16 kg.
Jakie są przeciwwskazania?
Nie stosować u zwierząt wykazujących nadwrażliwość na ceftiofur i inne antybiotyki beta-laktamowe.
Nie stosować w przypadku znanej oporności na substancję czynną.
Nie stosować w przypadku gdy wystąpiła oporność na inne cefalosporyny lub antybiotyki betalaktamowe.
Stosowanie produktu może prowadzić do wystąpienia przemijających dolegliwości w miejscu iniekcji.
Nie stosować u drobiu (również u niosek jaj konsumpcyjnych) z powodu ryzyka rozprzestrzenienia oporności na leki przeciwdrobnoustrojowe u ludzi.
Jakie są działania niepożądane?
Sporadycznie mogą pojawić się reakcje nadwrażliwości. W przypadku reakcji alergicznej leczenie powinno być przerwane.
U świń może się pojawić miejscowe podrażnienie w miejscu iniekcji i utrzymywać przez 5 lub więcej dni.
W przypadku zaobserwowania jakichkolwiek poważnych objawów lub innych objawów niewymienionych w ulotce informacyjnej, poinformuj o nich lekarza weterynarii.
Jakie są okres(-y) karencji?
Bydło: tkanki jadalne: 2 dni.
mleko: zero dni.
Świnie: tkanki jadalne: 2 dni.
Jakie są specjalne ostrzeżenia dla każdego z docelowych gatunków zwierząt?
Brak.
Jakie są specjalne ostrzeżenia dotyczące stosowania u zwierząt?
Stosowanie produktu w sposób odmienny od zaleceń podanych w ChPLW może prowadzić do wzrostu częstotliwości występowania bakterii opornych na ceftiofur i może obniżać skuteczność leczenia innymi cefalosporynami, z powodu możliwej oporności krzyżowej.
Bakteriobójcze właściwości β-laktamów są neutralizowane przez jednoczesne użycie antybiotyków bakteriostatycznych (makrolidów, sulfonamidów i tetracyklin).
U świń należy zachować szczególną ostrożność, aby uniknąć wstrzyknięcia w tkankę tłuszczową.
Należy unikać powtórnego wstrzykiwania w to samo miejsce iniekcji.
Produkt jest przeznaczony do leczenia pojedynczych zwierząt. Nie stosować zapobiegawczo ani w ramach programów ochrony zdrowia stad. Grupy zwierząt mogą być leczone zgodnie z warunkami określonymi w ChPL wyłącznie w przypadku stwierdzenia wybuchu choroby w stadzie.
Jakie są specjalne środki ostrożności dla osób podających Cefur zwierzętom?
Penicyliny i cefalosporyny mogą wywoływać reakcję nadwrażliwości (alergię) po wstrzyknięciu, wdychaniu, spożyciu lub kontakcie ze skórą. Nadwrażliwość na penicyliny może prowadzić do wystąpienia reakcji krzyżowych na cefalosporyny i odwrotnie. Reakcje alergiczne na te substancje sporadycznie mogą być poważne.
1. Osoby o znanej nadwrażliwości lub osoby, którym zalecono nie pracować z takimi produktami, nie powinny mieć kontaktu z tym produktem.
2. W celu uniknięcia narażenia z tym produktem należy obchodzić się bardzo ostrożnie, stosując się do wszystkich zalecanych środków ostrożności.
3. Jeśli po kontakcie z produktem pojawią się objawy takie jak wysypka na skórze, należy zwrócić się o pomoc lekarską i okazać lekarzowi niniejsze ostrzeżenia. Obrzęk twarzy, warg, powiek lub trudności z oddychaniem są poważniejszymi objawami i wymagają natychmiastowej pomocy lekarskiej.
Po użyciu należy umyć ręce.
Jak stosować Cefur w przypadku ciąży, laktacji lub nieśności?
Badania laboratoryjne u szczurów nie wykazały działania teratogennego, fetotoksycznego ani szkodliwego dla samicy.
Bezpieczeństwo produktu leczniczego weterynaryjnego nie zostało ocenione u bydła i świń w okresie ciąży i laktacji.
Do stosowania jedynie po dokonaniu przez lekarza weterynarii oceny bilansu korzyści/ryzyka wynikającego ze stosowania produktu.
Czy występują interakcje Cefur z innymi produktami?
–
Jak postępować w przypadku przedawkowania?
U bydła nie zaobserwowano objawów toksyczności ogólnej po przedawkowaniu.
U świń nie były obserwowane objawy toksyczności ogólnej po domięśniowym podawaniu dawki do 8-krotnie przekraczającej zalecaną, codziennie przez okres 15 dni.
Jakie są główne niezgodności farmaceutyczne?
Ponieważ nie wykonywano badań dotyczących zgodności, produktu leczniczego weterynaryjnego nie wolno mieszać z innymi produktami leczniczymi weterynaryjnymi.
Aktualna ulotka leku Cefur
Aktualna charakterystyka produktu leczniczego (ChPL)
Opinie, forum - zapoznaj się z doświadczeniami innych właścicieli zwierząt
Stosujesz Cefur u swojego pupila? Zachęcamy do podzielenia się opinią na jego temat na forum. Nie musisz się rejestrować, na poniższym formularzu wystarczy wpisanie nazwy użytkownika/pseudonimu.
Opisując doświadczenia na temat preparatu podawanemu zwierzęciu, możesz pomóc innym właścicielom zwierząt tych samych gatunków.